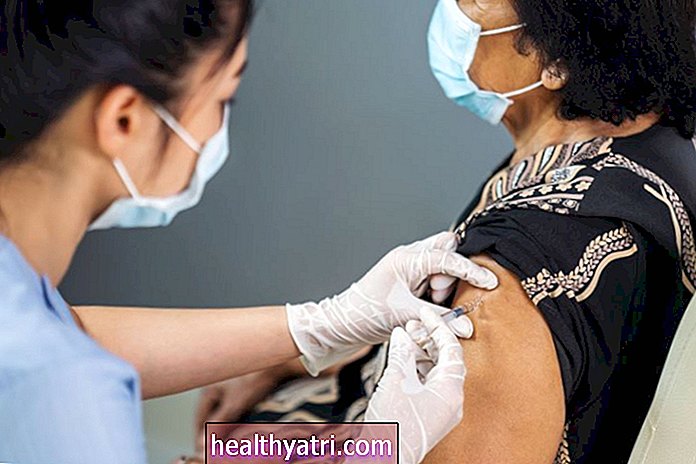
Digicomphoto / गेटी इमेजेज़
चाबी छीनना
- Vklury (remdesivir) COVID-19 वाले लोगों के लिए पहला FDA-अनुमोदित उपचार है।
- अनुमोदन केवल 88 पाउंड से ऊपर के अस्पताल में भर्ती मरीजों के लिए है।
- इससे पहले, दवा का FDA से आपातकालीन उपयोग प्राधिकरण था।
फूड एंड ड्रग एडमिनिस्ट्रेशन (एफडीए) ने अस्पताल में भर्ती मरीजों को 12 और इससे अधिक उम्र के सीओवीआईडी -19 के इलाज के लिए वेक्लेरी (रेमेडिसविर) को मंजूरी दे दी। यह COVID-19 की पहली आधिकारिक तौर पर FDA द्वारा अनुमोदित दवा है।
इससे पहले, एफडीए ने रीमेडिसविर के लिए आपातकालीन उपयोग प्राधिकरण (ईयूए) को मंजूरी दी थी, न कि पूर्ण अनुमोदन। 1 मई को जारी किए गए पहले ईयूए ने कहा कि अस्पताल में भर्ती मरीजों में गंभीर सीओवीआईडी -19 का रीमेडिसविर इस्तेमाल किया जा सकता है। यूरोपीय संघ ने 28 अगस्त को अस्पताल में भर्ती वयस्कों और बच्चों की पुष्टि या संदिग्ध मामलों की पुष्टि के लिए उनका उपयोग किया था, जो बीमारी की गंभीरता के बावजूद COVID-19 था।
हालांकि दवा अब अनुमोदित है, अनुमोदन सभी समूहों तक विस्तारित नहीं होता है। मरीजों को कम से कम 40 किलोग्राम (किग्रा) वजन घटाने के लिए 88 पाउंड वजन का होना चाहिए। जब आवश्यक हो, तो पहले यूरोपीय संघ के तहत कवर किए गए बाल रोगियों को दवा की पेशकश जारी रखने के प्रयास में, एफडीए ने फिर से जारी किया हैएक औरयूरोपीय संघ के लिए remdesiver उपयोग में:
- अस्पताल में भर्ती बाल रोगी, जिनका वजन 3.5 किलोग्राम से 40 किलोग्राम से कम है
- 12 वर्ष से कम आयु के अस्पताल में भर्ती बाल रोगी जिनका वजन कम से कम 3.5 किलोग्राम है
एफडीए आयुक्त स्टीफन एम। हैन ने एक बयान में कहा, "एफडीए इस अभूतपूर्व सार्वजनिक स्वास्थ्य आपातकाल के दौरान सीओवीआईडी -19 उपचार के विकास और उपलब्धता को बढ़ाने के लिए प्रतिबद्ध है।" “आज की स्वीकृति को कई नैदानिक परीक्षणों के डेटा द्वारा समर्थित है, जो एजेंसी ने कड़ाई से मूल्यांकन किया है और COVID-19 महामारी में एक महत्वपूर्ण वैज्ञानिक मील का पत्थर का प्रतिनिधित्व करता है। एफडीए के कोरोनावायरस ट्रीटमेंट एक्सेलेरेशन प्रोग्राम के हिस्से के रूप में, एजेंसी जल्द से जल्द रोगियों को नए चिकित्सा उत्पादों को स्थानांतरित करने में मदद करना जारी रखेगी, जबकि एक ही समय में यह निर्धारित करती है कि क्या वे प्रभावी हैं और यदि उनके लाभ उनके जोखिमों को कम करते हैं। "
Remdesivir क्या है?
रेमेड्सवियर एक प्रत्यक्ष अभिनय एंटीवायरल दवा है जो वायरल राइबोन्यूक्लिक एसिड (आरएनए) संश्लेषण को रोकता है। कोरोनवीरस, जिसमें एसएआरएस-सीओवी -2 शामिल है, एकल-फंसे हुए आरएनए एनोम का एक परिवार है। रेमेडीसविर इन वायरस को प्रतिकृति बनाने से रोकने के लिए सिद्ध हुआ है।
रेमेडिसविर और COVID-19
रेमेड्सवियर ने वसंत में पहली बार सुर्खियां बटोरीं, जब टेक्सास के शोधकर्ताओं ने सीमित नैदानिक आंकड़ों के बावजूद COVID-19 के लिए अंतःशिरा दवा को "सबसे होनहार चिकित्सा" के रूप में पहचाना।
जब SARS-CoV-2 उभरा, तो शोधकर्ताओं ने एक प्रयोगशाला में वायरस पर रेमेडिसविर का परीक्षण करने के बाद आशाजनक परिणाम देखे, और इसके कुछ ही समय बाद नैदानिक परीक्षण शुरू हुआ, मैथ्यू डी। हॉल, पीएचडी बताते हैं, जो नेशनल सेंटर फॉर एडवांस ट्रांसलेन्सिंग साइंसेज नेशनल में काम करता है। स्वास्थ्य संस्थान। उन्होंने COVID-19 OpenData पोर्टल को COVID-19 से संबंधित ड्रग रिप्रोज़िंग डेटा और प्रयोगों को सभी अनुमोदित दवाओं के लिए साझा करने में मदद की।
"अधिकांश अनुमोदित दवाओं को औसतन विकसित होने में 15 साल और कुछ बिलियन डॉलर लगते हैं," हॉल वेवेल्व बताता है। लेकिन हमें 15 साल नहीं हुए; हमारे पास 15 सप्ताह भी नहीं हैं। ”
हॉल का कहना है कि उन्हें और उनकी टीम को मौजूदा संसाधनों का मूल्यांकन करने का काम सौंपा गया था।
"हमें उन चीजों के लिए चारों ओर देखने की जरूरत है जो पहले से ही हमारे लिए उपलब्ध थीं जो या तो अन्य बीमारियों के इलाज के लिए अनुमोदित थीं या अन्य बीमारियों के इलाज के लिए विकसित की जा रही थीं," वे कहते हैं। "वे अभी तक अनुमोदित नहीं हो सकते हैं, लेकिन उम्मीद है कि वे मनुष्यों में रहे हैं और हम जानते हैं कि वे सुरक्षित हैं। हम बहुत भाग्यशाली हैं कि एंटीवायरल ड्रग्स के बहुत सारे हैं। उन दवाओं में से जो अनुमोदित हैं, या ड्रग उम्मीदवार, रेमेडिसविर प्रकट होते हैं। सबसे अधिक सक्रिय रहा है, यही कारण है कि इसे वास्तव में जल्दी से नैदानिक परीक्षणों में ले जाया जा सकता है। ”
मैथ्यू डी। हॉल, पीएचडी
अधिकांश अनुमोदित दवाओं को औसतन विकसित होने में 15 साल और कुछ अरब डॉलर लगते हैं। लेकिन हमारे पास 15 साल नहीं थे; हमारे पास 15 सप्ताह भी नहीं हैं।
- मैथ्यू डी। हॉल, पीएचडीएफडीए ने शुरू में 1 मई को यूरोपीय संघ को गंभीर COVID-19 के साथ वयस्क रोगियों को रेमिडीविर के साथ इलाज करने की अनुमति दी थी। गंभीर COVID-19 वाले व्यक्ति को इस रूप में परिभाषित किया गया था:
- 94% से कम या बराबर ऑक्सीजन संतृप्ति वाला एक रोगी
- पूरक ऑक्सीजन की आवश्यकता वाले एक रोगी
- एक मरीज को मैकेनिकल वेंटिलेशन की आवश्यकता होती है
- एक मरीज को एक्स्ट्राकोर्पोरियल झिल्ली ऑक्सीजनेशन की आवश्यकता होती है
विस्तारित EUA ने पहले चरण में या रोग के मामूली मामलों के साथ रोगियों को दवा उपलब्ध कराने में मदद की, और अनुमोदन केवल इसकी उपलब्धता को बढ़ाना चाहिए। हॉल का कहना है कि रोगियों को उपचार प्राप्त करने के लिए एक नैदानिक पथ के भाग के रूप में पंजीकृत होने की आवश्यकता नहीं है, जो ग्रामीण समुदायों में रहने वाले लोगों तक पहुंच बढ़ाता है जो अनुसंधान सुविधाओं के पास नहीं रहते हैं।
"मुझे लगता है कि हम सभी सहमत हैं कि यह उन लोगों के लिए अच्छा होगा जो घर पर थोड़े अस्वस्थ हैं, जल्द ही अपने शरीर से वायरस को मिटाने के लिए एक एंटीवायरल ले सकते हैं ताकि यह सुनिश्चित हो सके कि वे बाद में बीमार नहीं होंगे," हॉल कहते हैं। "अभी, आपको तब तक इंतजार करना होगा जब तक आप अस्पताल में भर्ती होने के लिए पर्याप्त नहीं होंगे। यह सुनिश्चित करने के लिए बहुत अच्छा होगा कि वे लोग कभी बीमार नहीं होंगे जो पहले अस्पताल में जाने के लिए उन्हें एंटीवायरल देकर फ्लू के लिए टैमीफ्लू की तरह देते हैं, (जहां आप डॉक्टर के पास जाते हैं, गोली ले लेते हैं और यह आपके समय को छोटा कर देगा) के लिए फिर से बीमार
रेमेडिसविर का विकास
रेमेड्सविर को शुरू में गिलियड साइंसेज, यू.एस. सेंटर्स फॉर डिजीज कंट्रोल एंड प्रिवेंशन और यू.एस. आर्मी मेडिकल रिसर्च इंस्टीट्यूट ऑफ इंफेक्शियस डिजीज के बीच सहयोग के रूप में विकसित किया गया था। यह पश्चिम अफ्रीकी इबोला वायरस महामारी के दौरान और दो अन्य कोरोनवीरस के लिए संभावित चिकित्सीय के रूप में पता लगाया गया था: गंभीर तीव्र श्वसन सिंड्रोम (SARS) और मध्य पूर्व श्वसन सिंड्रोम (MERS)।
कौन रेमेडिसवीर लेना चाहिए?
रेमेडिसविर की इष्टतम रोगी आबादी, खुराक और उपचार की अवधि ज्ञात नहीं है। स्वास्थ्य सेवा प्रदाताओं के लिए एक तथ्य पत्र में, FDA निम्नलिखित सिफारिशें प्रदान करता है:
- 40 किलोग्राम और अधिक वजन वाले वयस्कों और बाल रोगियों के लिए, अनुशंसित खुराक दिन 1 पर 200 मिलीग्राम और बाद में 100 मिलीग्राम की खुराक है।
- 3.5 किलोग्राम और 40 किलोग्राम के बीच वजन वाले बाल रोगियों के लिए, अनुशंसित खुराक 1 दिन में 5 मिलीग्राम / किग्रा है और बाद में 2.5 मिलीग्राम / किग्रा की खुराक लेती है।
- रोगियों को इनवेसिव मैकेनिकल वेंटिलेशन और / या एक्स्ट्राकोर्पोरियल मेम्ब्रेन ऑक्सीजनेशन की आवश्यकता नहीं होती है, इसके लिए कुल ट्रीटमेंट की अवधि 5 दिन है।
- इनवेसिव मैकेनिकल वेंटिलेशन और / या एक्स्ट्राकोर्पोरियल मेम्ब्रेन ऑक्सीजनेशन की आवश्यकता वाले रोगियों के लिए, उपचार की कुल अवधि 10 दिन है।
- यदि कोई रोगी नैदानिक सुधार का प्रदर्शन नहीं करता है, तो उपचार को 10 दिनों तक की कुल उपचार अवधि के लिए 5 अतिरिक्त दिनों तक बढ़ाया जा सकता है।
गिलियड साइंसेज, रेमेडिसविर के उत्पादन और वितरण को बढ़ाने के लिए काम कर रहा है, जिसे एक जांच दवा माना जाता है और वर्तमान में इसके संकेत के लिए अनुमोदित नहीं किया जाता है।
नैदानिक परीक्षण और प्रारंभिक खोजें
एफडी का निर्णय रेमेडिसविर को मंजूरी देने के लिए कुछ नैदानिक परीक्षणों से शोध के निष्कर्षों पर आधारित है, और इसे चिकित्सा समुदाय से मिश्रित राय के साथ मिला है।
"मैं किसी भी दवा या किसी भी दवा उम्मीदवार के बारे में क्या सोचता हूं, यह वास्तव में मायने नहीं रखता है," हॉल कहते हैं। “क्या वास्तव में मायने रखता है एक अच्छी तरह से नियंत्रित नैदानिक परीक्षण से डेटा है। यदि वे सोचते हैं कि अधिक रोगियों के लिए लाभ होगा, तो FDA ने EUA का दायरा नहीं बढ़ाया होगा।
29 अप्रैल को प्रकाशित एक अध्ययन मेंनश्तर,चिकित्सकों और शोधकर्ताओं के एक समूह ने चीन के हुबेई में 10 अस्पतालों में गंभीर सीओवीआईडी -19 के साथ 237 वयस्क रोगियों का यादृच्छिक, डबल-अंधा, प्लेसबो-नियंत्रित परीक्षण किया।
"हालांकि सांख्यिकीय रूप से महत्वपूर्ण नहीं है, रेमेडिसविर प्राप्त करने वाले रोगियों के पास नैदानिक सुधार के लिए संख्यात्मक रूप से तेज समय था, जो कि 10 दिनों या उससे कम के लक्षणों वाले रोगियों में प्लेसबो प्राप्त करते हैं," लेखक लिखते हैं।
अमेरिकी सरकार द्वारा प्रायोजित अध्ययन ने 22 मई को अपने प्रारंभिक निष्कर्ष प्रकाशित किएन्यू इंग्लैंड जर्नल ऑफ मेडिसिन1,063 COVID-19 रोगियों के यादृच्छिक, डबल-ब्लाइंड प्लेसबो-नियंत्रित परीक्षण से। शोधकर्ताओं ने पाया कि उन लोगों ने रेमेडिसविर का 10 दिन का कोर्स सौंपा था, जिसमें प्लेसबो की तुलना में रिकवरी का समय कम था - 11 बनाम 15 दिनों का माध्य।
"ये प्रारंभिक निष्कर्ष COVID-19 के साथ अस्पताल में भर्ती मरीजों और पूरक ऑक्सीजन थेरेपी की आवश्यकता के लिए रेमेडिसविर के उपयोग का समर्थन करते हैं," लेखक लिखते हैं। "हालांकि, रेमेडिसविर के उपयोग के बावजूद उच्च मृत्यु दर दी गई है, यह स्पष्ट है कि अकेले एक एंटीवायरल दवा के साथ उपचार पर्याप्त होने की संभावना नहीं है।"
21 अगस्त को,अमेरिकन मेडिकल एसोसिएशन के जर्नल584 रोगियों के एक यादृच्छिक चरण -3 के परीक्षण को मध्यम COVID-19 निमोनिया के साथ अस्पताल में भर्ती कराया गया। रेमेडिसविर निर्माता गिलियड साइंसेज ने संयुक्त राज्य अमेरिका, यूरोप और एशिया के 105 अस्पतालों में इस परीक्षण को प्रायोजित किया। मरीजों को रीमेडिसविर का 5-दिन या 10-दिवसीय पाठ्यक्रम प्राप्त हुआ या उन्हें मानक देखभाल दी गई। शोधकर्ताओं ने 10-दिवसीय समूह के परिणामों में कोई अंतर नहीं पाया, और 5-दिवसीय समूह के बीच थोड़ा सार्थक अंतर पाया।
सभी तीनों अध्ययनों में अलग-अलग सीमाएँ थीं और उनमें महत्वपूर्ण अंतर था, इसलिए तुलनात्मक रूप से एक सेब बनाना उचित नहीं था। हालाँकि, यह निष्कर्षों के बारे में सवाल उठाता है, नैदानिक अनुसंधान की एक बानगी।
"अब अलग-अलग परिणामों के साथ अस्पताल में भर्ती मरीजों में रेमेडिसविर के तीन [यादृच्छिक नियंत्रण परीक्षण] हैं, इस सवाल को उठाते हुए कि क्या विसंगतियां अध्ययन डिजाइन विकल्पों की कलाकृतियों हैं, जिसमें रोगी आबादी भी शामिल है, या क्या दवा आशा से कम प्रभावकारी है," विश्वविद्यालय पिट्सबर्ग स्कूल ऑफ मेडिसिन के शोधकर्ताओं ने एक संपादकीय में लिखाअमेरिकन मेडिकल एसोसिएशन के जर्नल21 अगस्त को, "इसलिए यह अवशिष्ट अनिश्चितताओं को दूर करने और इष्टतम उपयोग को सूचित करने के लिए डिज़ाइन किए गए बड़े पैमाने पर यादृच्छिक नियंत्रण परीक्षणों में रेमेडिसविर के तत्काल मूल्यांकन करने के लिए विवेकपूर्ण लगता है।"
यह आपके लिए क्या मायने रखता है
अमेरिकी खाद्य एवं औषधि प्रशासन ने रेमेडिसविर को अपनी पहली COVID-19 उपचार स्वीकृति प्रदान कर दी है। यदि आपको COVID-19 की पुष्टि या संदिग्ध मामले के साथ अस्पताल में भर्ती कराया जाता है, तो आपका स्वास्थ्य सेवा प्रदाता इस दवा को निर्धारित करने का निर्णय ले सकता है।
Remdesivir के लिए आगे क्या है?
गिलियड साइंसेज वेबसाइट के अनुसार, अधिक नैदानिक परीक्षण चल रहे हैं। कंपनी इनहेलर के रूप में रेमेडिसविर तैयार करने के लिए विकास के पहले चरण में भी है।
हॉल का कहना है कि वैश्विक समुदाय चुनौती के लिए बढ़ गया है, लेकिन SARS-CoV-2 के लिए एक दवा की खोज को इस तथ्य से जटिल किया गया है कि मानव कोरोनवीयरस के लिए कोई चिकित्सीय नहीं हैं। हाल ही में SARS और MERS का प्रकोप जन स्वास्थ्य उपायों के माध्यम से लड़ा गया था, न कि चिकित्सीय।
हॉलिडे का कहना है, "रेमिडीविर के साथ, हम सुपर भाग्यशाली हैं।" "हम भाग्यशाली हैं कि इसे इबोला के लिए विकसित किया जा रहा था। हम भाग्यशाली हैं कि यह अब मनुष्यों में परीक्षण के लिए उपलब्ध था। क्योंकि यदि आप समीकरण से रेमेडिसविर को घटाते हैं, तो मुझे नहीं पता कि अगली सबसे अच्छी बात क्या है।" अन्य दवा SARS-CoV-2 संक्रमण के इलाज के लिए अनुमोदित है। ”